中國蘇州和美國馬里蘭州羅克維爾市2021年1月14日—致力于在腫瘤、乙肝及與衰老相關(guān)疾病等治療領(lǐng)域開發(fā)創(chuàng)新藥物的處于臨床階段的研發(fā)企業(yè)-- 亞盛醫(yī)藥(6855.HK)于北京時間1月13日晚間出席第39屆摩根大通醫(yī)療(線上)官方會議���。亞盛醫(yī)藥董事長����、CEO楊大俊博士代表公司匯報近期多項進展,全球創(chuàng)新價值凸顯����。
全球創(chuàng)新進展頻頻
楊大俊博士就公司研發(fā)管線與近期業(yè)務(wù)進展作了精彩報告。作為全球領(lǐng)先的蛋白-蛋白相互作用靶點藥物研發(fā)公司��,公司擁有極具國際競爭力的產(chǎn)品管線��,在研項目多具有全球性“first-in-class”或“best-in-class”潛力(見表1)����。目前亞盛醫(yī)藥已獲得臨床批件33項,正在全球?qū)用骈_展40多項臨床研究����。
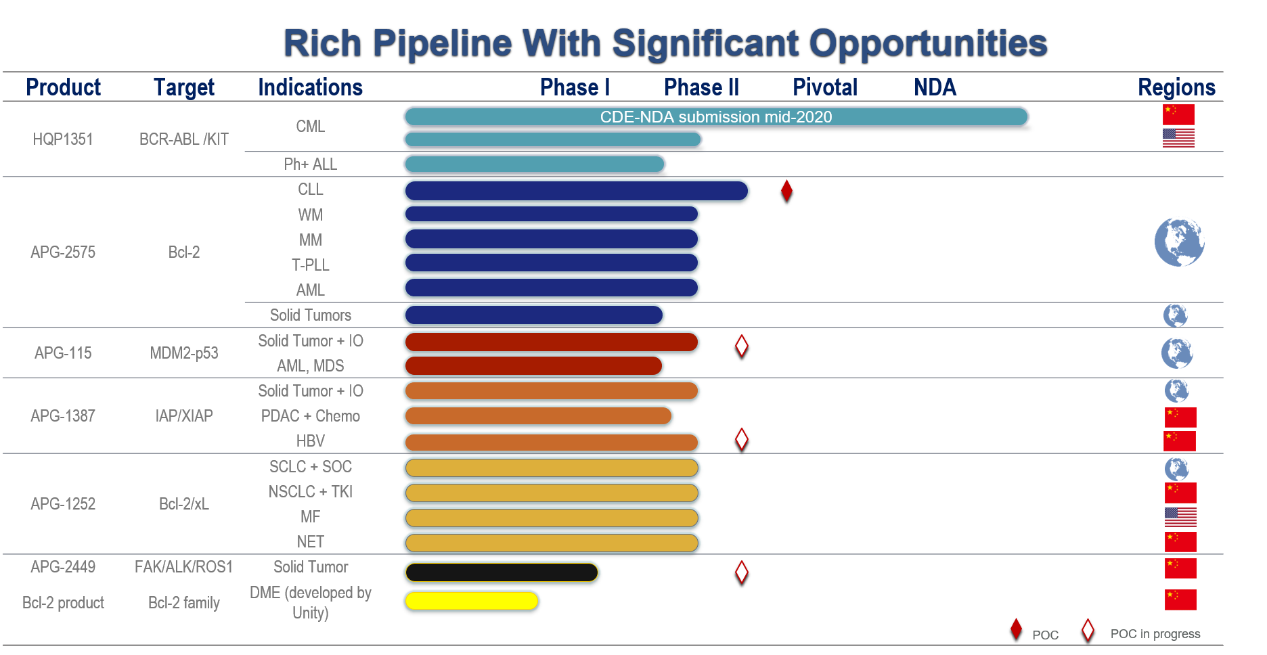
表1 公司主要產(chǎn)品管線圖
楊大俊博士特別總結(jié)了公司2020年在新冠疫情的挑戰(zhàn)下依舊取得的眾多里程碑式進展:
Bcl-2抑制劑APG-2575呈現(xiàn)明顯優(yōu)勢與潛力
作為全球領(lǐng)先的細胞凋亡通路新藥研發(fā)公司,亞盛醫(yī)藥在該領(lǐng)域已構(gòu)建豐富的品種布局����,并針對Bcl-2、IAP 及MDM2-p53 三條關(guān)鍵細胞凋亡路徑推進5個在研品種進入臨床階段。其中APG-2575為公司自主研發(fā)的新型口服Bcl-2選擇性小分子抑制劑�,是全球?qū)用胬^Venetoclax之后罕有的進入臨床開發(fā)階段的Bcl-2選擇性抑制劑,也是首個在中國進入臨床階段的���、本土研發(fā)的Bcl-2選擇性抑制劑����,備受關(guān)注��。
2020年12月�,公司已公布APG-2575的最新臨床進展:針對復(fù)發(fā)/難治CLL的臨床研究已入組30多位患者,初步臨床研究結(jié)果顯示��,在可評估患者中的客觀緩解率(ORR)達到70%�����。這一數(shù)據(jù)非常令人振奮����。在本次摩根大通會議上,楊大俊博士進一步展示了相關(guān)數(shù)據(jù)�。
特別是在APG-2575的有效性方面,楊大俊博士強調(diào)了兩點���,一是在重要的有效性指標(biāo)淋巴細胞絕對數(shù)(ALC)方面��,3位高風(fēng)險的入組患者在接受一個周期的治療之后�,ALC指標(biāo)已經(jīng)恢復(fù)正常的水平(見圖1)����;二是在相較基線的淋巴結(jié)體積方面,可評估患者的變化非常明顯 (見圖2)�。
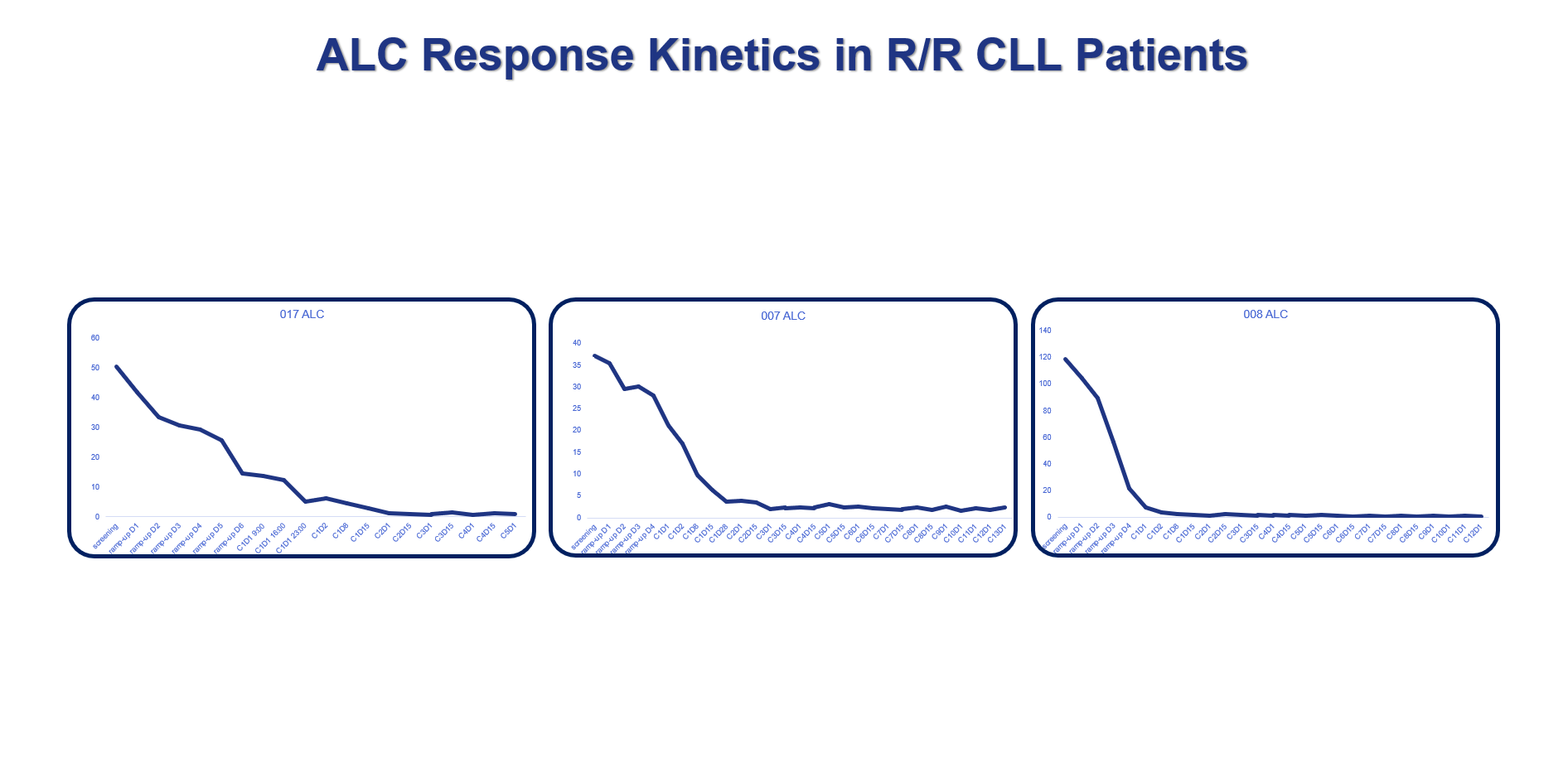
圖1
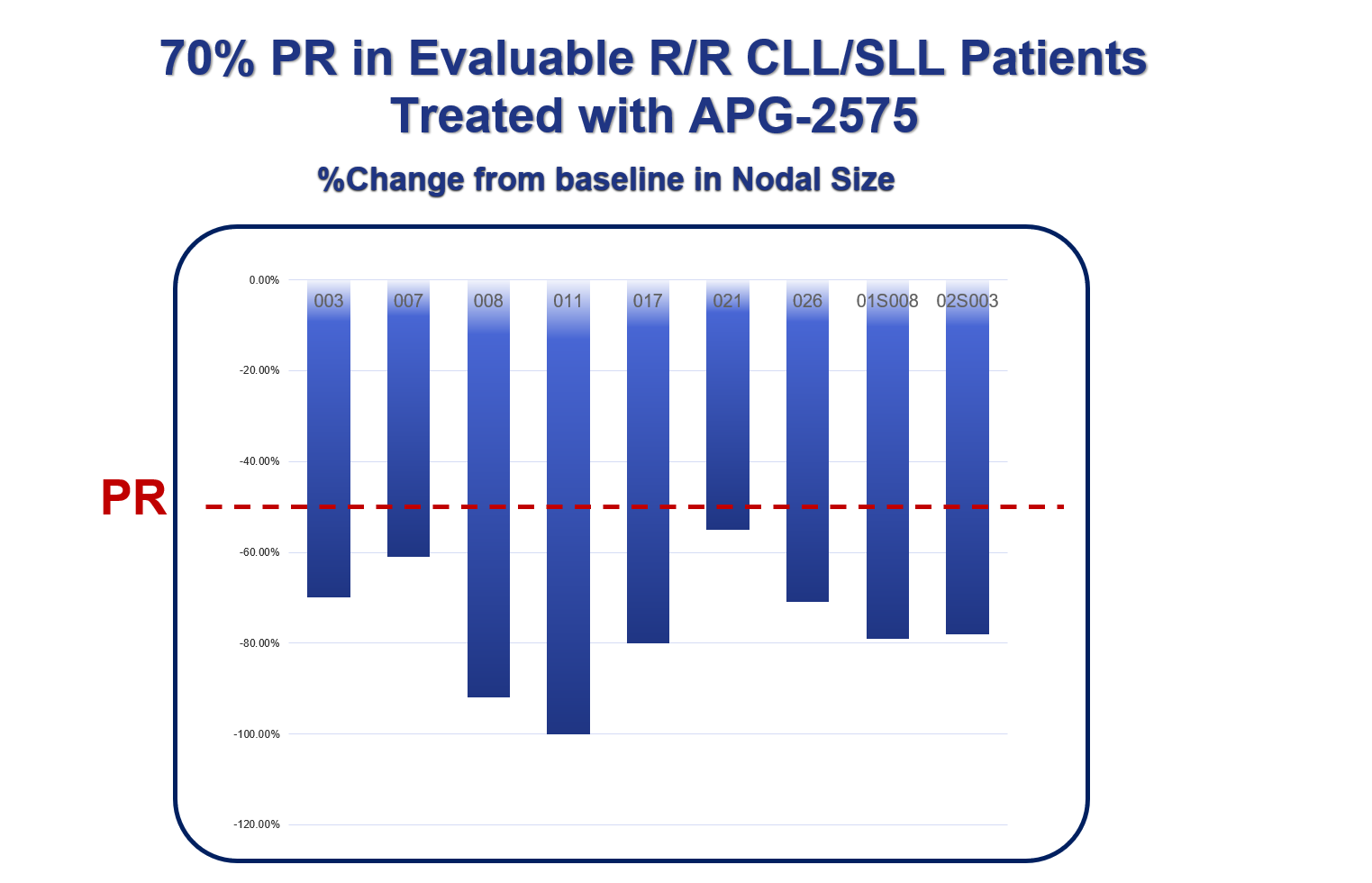
圖2
Figure 2
同時�,楊大俊博士還指出��,臨床前數(shù)據(jù)顯示�,APG-2575在BTK耐藥��、Venetoclax 無效的WM PDX模型中顯示良好的抑制腫瘤效果(見圖3)�����。這為APG-2575臨床適應(yīng)癥的進一步探索提供了基礎(chǔ)�����,顯示較大潛力�。
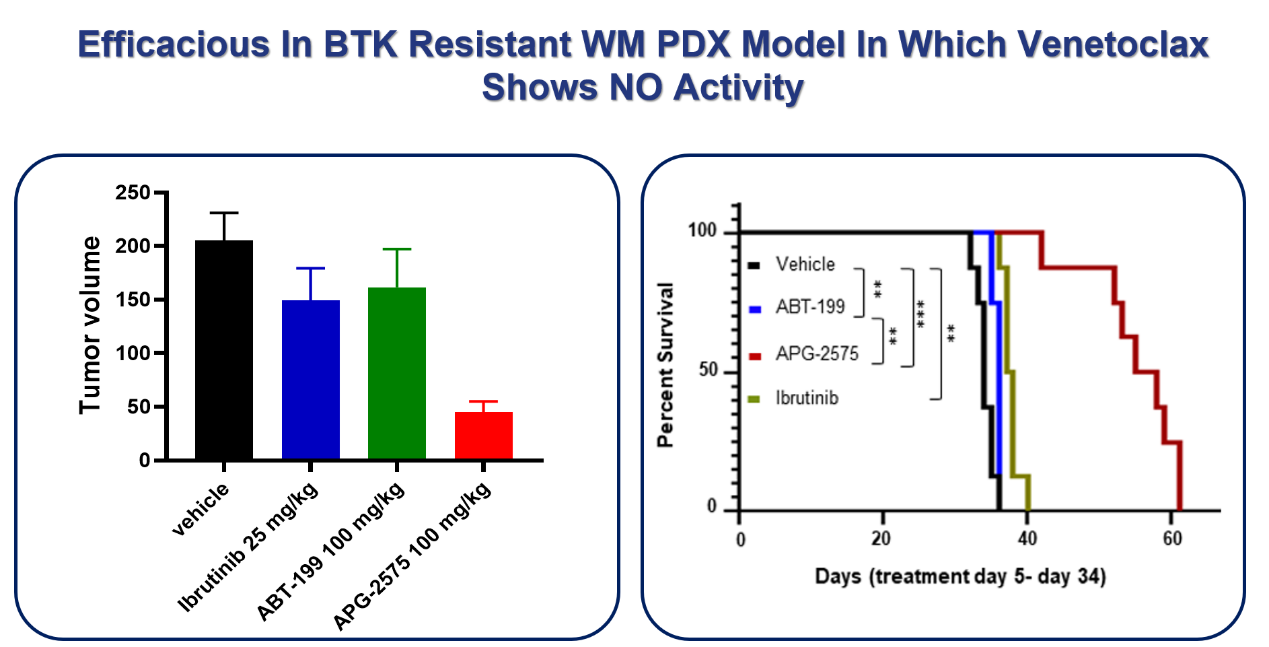
圖3
楊大俊博士表示:很高興能受邀參加本屆摩根大通醫(yī)療大會����,與全球的醫(yī)藥投資者分享我們的近期進展����。整體而言��,在全球新冠疫情的挑戰(zhàn)下��,亞盛在2020年仍獲得多項里程碑進展�,我們的“全球創(chuàng)新”的戰(zhàn)略效應(yīng)逐步顯現(xiàn)。我們將繼續(xù)堅持這一戰(zhàn)略�����,加快全球?qū)用娴呐R床開發(fā),進一步壘實公司在細胞凋亡新藥研發(fā)的領(lǐng)先地位��,并早日將產(chǎn)品推向上市�����?!?/span>
關(guān)于亞盛醫(yī)藥
亞盛醫(yī)藥是一家立足中國����、面向全球的處于臨床開發(fā)階段的原創(chuàng)新藥研發(fā)企業(yè),致力于在腫瘤����、乙肝及與衰老相關(guān)的疾病等治療領(lǐng)域開發(fā)創(chuàng)新藥物。2019年10月28日�����,亞盛醫(yī)藥在香港聯(lián)交所主板掛牌上市���,股票代碼:6855.HK��。
亞盛醫(yī)藥擁有自主構(gòu)建的蛋白-蛋白相互作用靶向藥物設(shè)計平臺�,處于細胞凋亡通路新藥研發(fā)的全球最前沿�。公司已建立擁有8個已進入臨床開發(fā)階段的1類小分子新藥產(chǎn)品管線,包括抑制Bcl-2���、IAP 或 MDM2-p53 等細胞凋亡路徑關(guān)鍵蛋白的抑制劑�;新一代針對癌癥治療中出現(xiàn)的激酶突變體的抑制劑等��,為全球唯一在細胞凋亡路徑關(guān)鍵蛋白領(lǐng)域均有臨床開發(fā)品種的創(chuàng)新公司�����。目前公司正在中國��、美國及澳大利亞開展40多項I/II期臨床試驗�����。用于治療耐藥性慢性髓性白血病的核心品種HQP1351已在中國遞交新藥上市申請����,該品種獲得了美國FDA審評快速通道及孤兒藥認證資格。截至目前�,公司共有4個在研新藥獲得9項FDA孤兒藥資格認證��。
前瞻性聲明
本文所作出的前瞻性陳述僅與本文作出該陳述當(dāng)日的事件或資料有關(guān)���。除法律規(guī)定外,于作出前瞻性陳述當(dāng)日之后�����,無論是否出現(xiàn)新資料�、未來事件或其他情況,我們并無責(zé)任更新或公開修改任何前瞻性陳述及預(yù)料之外的事件����。請細閱本文,并理解我們的實際未來業(yè)績或表現(xiàn)可能與預(yù)期有重大差異����。本文內(nèi)所有陳述乃本文章刊發(fā)日期作出,可能因未來發(fā)展而出現(xiàn)變動�。