近日���,思路迪醫(yī)藥(3D Medicines, 01244.HK)宣布���,公司在研候選藥物3D189(galinpepimut-S����,GPS)單藥治療經(jīng)挽救治療后獲得第二次完全緩解的急性髓性白血?��。ˋML)患者的 III 期全球多中心臨床試驗(yàn)(MRCT)已獲國家藥品監(jiān)督管理局(NMPA)的臨床試驗(yàn)許可�。此前�,3D189在國外已有多項(xiàng)的 I、II 期臨床研究完成�����,該MRCT研究(SLG18-301)正在美國和歐洲開展��。這是一項(xiàng)開放性�����、多中心�、隨機(jī)、平行對(duì)照研究���,預(yù)計(jì)將招募約116名患者�,在全球約110個(gè)研究中心進(jìn)行。本次關(guān)鍵研究臨床試驗(yàn)方案獲批��,是3D189于國內(nèi) I 期評(píng)估安全耐受性和免疫原性試驗(yàn)基礎(chǔ)上的第二項(xiàng)臨床試驗(yàn)?zāi)驹S可����。3D189是思路迪醫(yī)藥第三款進(jìn)入 III 期臨床的重磅產(chǎn)品,此次臨床獲批加快了產(chǎn)品獲批上市的步伐�。3D189有望減少多種腫瘤復(fù)發(fā)轉(zhuǎn)移�����,從而延長腫瘤患者生存期����,提高生活質(zhì)量。
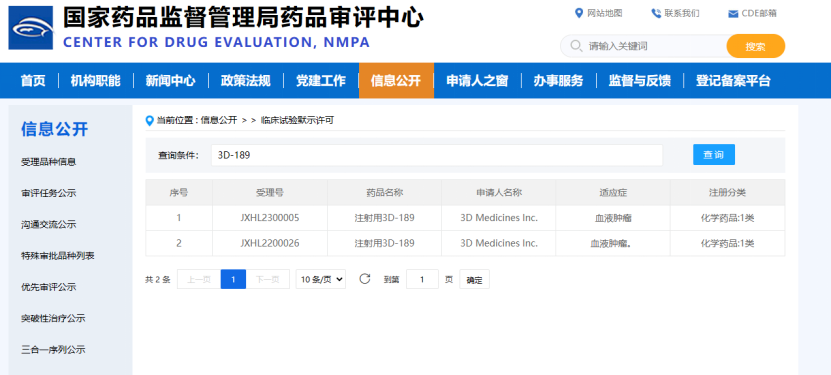
3D189是一種針對(duì)WT1(Wilms Tumor 1)蛋白的腫瘤疫苗�,由4條多肽鏈組成,能夠識(shí)別并結(jié)合25個(gè)抗原表位�����,激發(fā)自身免疫系統(tǒng)產(chǎn)生強(qiáng)烈的免疫反應(yīng)��,以達(dá)到殺死癌細(xì)胞和增強(qiáng)免疫系統(tǒng)對(duì)癌細(xì)胞的監(jiān)測作用,并在緩解期時(shí)對(duì)殘留的癌細(xì)胞產(chǎn)生顯著的治療效果����。WT1是廣泛表達(dá)的癌癥抗原之一,被美國國家癌癥研究所(NCI)列為癌癥免疫治療的首要靶標(biāo)�。此外,由于WT1蛋白在多種血液惡性腫瘤和實(shí)體腫瘤細(xì)胞中過度表達(dá)��,而在正常成人組織中表達(dá)很少�,因此靶向WT1的癌癥疫苗具有廣泛應(yīng)用的潛力且安全性良好。3D189前期由美國紀(jì)念斯隆-凱特琳癌癥中心(MSKCC)和SELLAS Life Sciences Group, Inc.(SELLAS)開發(fā)��。思路迪醫(yī)藥于2020年12月8日與SELLAS達(dá)成合作�,獲得3D189在大中華區(qū)所有適應(yīng)癥的獨(dú)家開發(fā)及商業(yè)化權(quán)利。本品已在多個(gè)腫瘤適應(yīng)癥中開展臨床試驗(yàn)����,包括急性髓性白血病(AML)�、惡性胸膜間皮瘤(MPM)、多發(fā)性骨髓瘤(MM)���、卵巢癌等��。已經(jīng)完成AML患者首次完全緩解的 II 期試驗(yàn)�����,結(jié)果顯示����,維持治療環(huán)境接受3D189治療,在老年患者(>60歲)中���,中位總生存期達(dá)到35.3個(gè)月�����,在所有年齡段的患者中達(dá)到67.6個(gè)月。觀察到令人信服的CD4和CD8反應(yīng)性����。3D189單藥治療在前期多項(xiàng)試驗(yàn)中表現(xiàn)出良好的安全性及初步有效性,已獲得兩項(xiàng)FDA快速通道資格認(rèn)定��。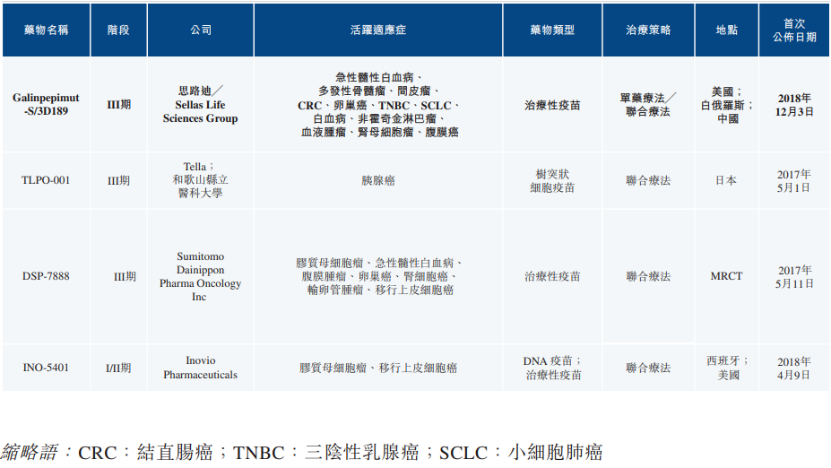
已有臨床數(shù)據(jù)表明��,3D189能夠在低腫瘤負(fù)荷環(huán)境下誘發(fā)抗腫瘤免疫應(yīng)答以及加強(qiáng)免疫監(jiān)視����;免疫檢查點(diǎn)抑制劑在大量臨床數(shù)據(jù)中(如抗PD-L1的單域恩維達(dá)?)展示出抑制免疫逃逸的能力,使得細(xì)胞毒性T細(xì)胞能滲透腫瘤及造成人類惡性腫瘤擴(kuò)大集群中的腫瘤消退。I/II 期研究數(shù)據(jù)的最終分析結(jié)果(SLS17-201/MK3475-770�����;NCT03761914)���,表明GPS與PD-1抗體pembrolizumab(Keytruda?)的組合似乎能夠減緩疾病進(jìn)展����,而對(duì)于在經(jīng)治后復(fù)發(fā)的可測耐鉑卵巢癌癥患者��,其平均總生存期超過18個(gè)月���。3D189聯(lián)合恩維達(dá)?被推定能夠增加激活免疫應(yīng)答��,并引入記憶T細(xì)胞延長該應(yīng)答的持續(xù)時(shí)間�����。此外����,3D189與恩維達(dá)?同樣能夠進(jìn)行便捷的皮下注射����,因此��,聯(lián)合使用有望產(chǎn)生良好的協(xié)同效應(yīng)�����。3D189是一種靶向WT1的創(chuàng)新性腫瘤免疫治療新藥��,在過度表達(dá)WT1蛋白的超過20種癌癥(包括肺癌及直腸癌)中具備靶向治療潛質(zhì)�,可誘導(dǎo)產(chǎn)生強(qiáng)大的T細(xì)胞介導(dǎo)的免疫應(yīng)答的刺激作用����,用于預(yù)防/延遲復(fù)發(fā)(通過延長無疾病進(jìn)展期)及最終有望延長患者的生存期。? ?3D189適用于全球范圍內(nèi)絕大多數(shù)人類白細(xì)胞組織兼容性抗原(HLA)類型�,可作為單藥用于低腫瘤負(fù)荷臨床情況下(如AML完全緩解患者)的維持治療,也可與PD-1/PD-L1抗體等其他抗腫瘤藥物聯(lián)合用藥提高療效�。關(guān)于思路迪醫(yī)藥(3D Medicines Inc.)思路迪醫(yī)藥是一家進(jìn)入商業(yè)化階段專注腫瘤治療領(lǐng)域的創(chuàng)新藥公司�,秉承“幫助腫瘤患者活得更久更好”的愿景,針對(duì)腫瘤治療慢病化趨勢開發(fā)抗腫瘤藥物���。公司于2022年12月15日正式登陸香港交易所主板�,股票簡稱:3D Medicines- B����,股票代碼:1244��。公司產(chǎn)品線包括12款具有臨床價(jià)值的創(chuàng)新藥�,其中8款已進(jìn)入臨床開發(fā)或商業(yè)化階段�,包括皮下注射PD-L1單域抗體新藥恩維達(dá)?已獲國家藥品監(jiān)督管理局批準(zhǔn)上市銷售;引進(jìn)多肽腫瘤疫苗3D189和GAS6/AXL抑制劑3D229已進(jìn)入全球 III 期臨床研究�;自主研發(fā)的多靶點(diǎn)激酶抑制劑3D011也進(jìn)入了臨床開發(fā)階段,臨床前品種包括國際領(lǐng)先的雙抗CD3xPD-L1等�。公司建立了完善的創(chuàng)新藥研發(fā)平臺(tái),涵蓋腫瘤靶點(diǎn)驗(yàn)證���、藥物發(fā)現(xiàn)�、生物標(biāo)志物開發(fā)以及臨床開發(fā)等�����。公司逾200人的國際化團(tuán)隊(duì)����,具有從藥物發(fā)現(xiàn)、臨床前研究�、臨床開發(fā)、申報(bào)上市及商業(yè)化的成功經(jīng)驗(yàn)����,多個(gè)適應(yīng)癥已獲得FDA及NMPA孤兒藥認(rèn)證或優(yōu)先審評(píng)����。思路迪醫(yī)藥秉承以臨床價(jià)值為中心�����,為全球腫瘤患者開發(fā)更優(yōu)的腫瘤治療藥物�。更多信息請(qǐng)?jiān)L問:http://www.3d-medicines.com