4月11日���,據(jù)國家藥監(jiān)局公示��,智核生物持有的人促甲狀腺素注射液(通用名人促甲狀腺激素注射液����,商品名智舒嘉?)獲批上市,適應癥為用于無遠處轉移的分化型甲狀腺癌患者在甲狀腺全切或近全切除術后碘[131I]清除殘余甲狀腺組織的輔助治療���。該產品為創(chuàng)新預充水針劑型����,注冊分類為2.1類改良型新藥���,為國內首個上市的重組人促甲狀腺激素(rhTSH)�����。
NMPA官網
據(jù)國家癌癥中心估算數(shù)據(jù)�����,我國2022年甲狀腺癌年新發(fā)病例為46.6萬,在各類惡性腫瘤中排名第3位�;其中,分化型甲狀腺癌是甲狀腺癌的主要類型��,占比高達95%以上����。全國平均發(fā)病率為14.6/10萬,城市地區(qū)高發(fā)�,北上廣深的發(fā)病率高達40-50/10萬。近10年�,女性人群甲狀腺癌的發(fā)病每年增幅超過20%。我國甲狀腺癌5年生存率84.3%�,遠低于美國的98.3%。
圖:中國甲狀腺癌發(fā)病率�����、中美甲狀腺癌5年生存率
甲狀腺手術治療+術后碘131治療+促甲狀腺激素(TSH)抑制治療�,是分化型甲狀腺癌治療的標準方法。全切或近全切手術后的分化型甲狀腺癌患者疾病狀態(tài)的實時評估前及碘131治療前準備前���,均需升高體內TSH水平���,達到刺激甲狀腺球蛋白分泌和促進碘131攝取的目的,從而更好地評估病情或提高碘131治療療效��。
圖:分化型甲狀腺癌治療三部曲
升高體內促甲狀腺激素水平的方式主要有兩種:一是傳統(tǒng)甲狀腺激素撤退(THW)方式����,即停服左甲狀腺素鈉片(L-T4)2-4周,二是給予外源性的rhTSH�。
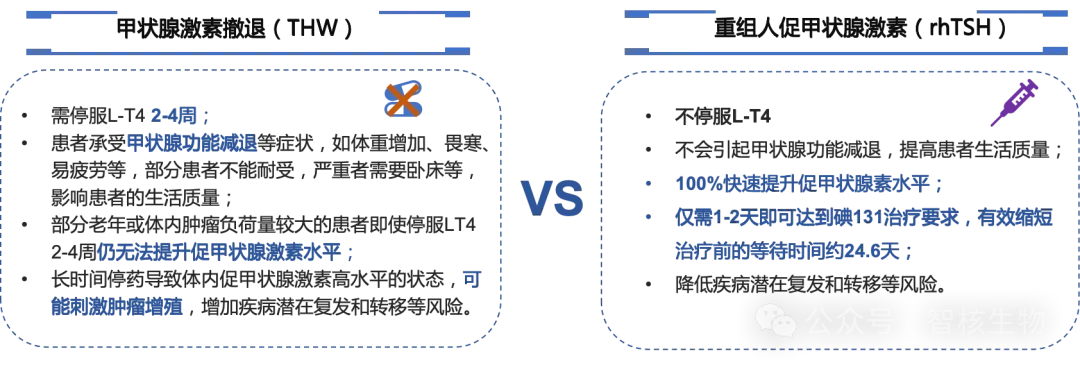
此前��,由于國內沒有rhTSH類藥物��,碘131治療前提升TSH只能采用停服L-T4的方式��,患者需要承受停服L-T4導致的甲狀腺功能減退帶來的各種不適����,面臨潛在的病灶增殖風險等。此外����,全國核醫(yī)學科核素治療病床數(shù)量有限,應用rhTSH可以避免患者可能發(fā)生的停服L-T4后TSH仍無法達標�����,從而導致提前預約好的床位空置的情況����;也可幫助不能耐受甲減癥狀的患者高質量地接受治療,幫助核醫(yī)學科高效率的運轉核素治療床位��,緩解醫(yī)療資源緊張的狀態(tài)���,全方面滿足醫(yī)生和患者的臨床需求����。
圖:智舒嘉圖片
據(jù)悉�����,重組人促甲狀腺激素最早于1998年在美國上市��,由健贊Genzyme公司生產�,目前已在包括中國臺灣和香港的60多個國家和地區(qū)銷售,但未進入大陸市場���。近30年的臨床應用經驗使這類藥物獲得了國內外多個甲狀腺癌相關的指南推薦�。此次智核生物人促甲狀腺素注射液的上市將填補中國大陸該領域用藥空白�。
智核生物人促甲狀腺素注射液,商品名為智舒嘉?����,其主要成分為重組人促甲狀腺激素(rhTSH),是一種與人體內垂體分泌的促甲狀腺激素(TSH)為同類糖蛋白����,可在首次注射48小時內100%快速提升患者體內促甲狀腺激素水平,促進碘攝取和有機化�,便于分化型甲狀腺癌患者快速接受碘治療;此外,rhTSH能夠刺激體內殘留的甲狀腺組織或轉移灶分泌甲狀腺球蛋白��,便于診斷及監(jiān)測疾病進展�。
2018年早期臨床試驗研究顯示,該藥物不良反應輕微��,安全耐受性良好�����。2019年12月起�,智核生物人促甲狀腺素注射液在全國19家研究中心開展III期臨床試驗,累計納入受試者307例��。結果顯示其療效非劣效于目前臨床實踐中常用且唯一的停服甲狀腺素法���,智舒嘉組體內促甲狀腺激素水平3天內即達標�,明顯快于THW組�����;且安全耐受性良好�����,有效降低不良反應發(fā)生率,具有明確的臨床需求和價值����。
蘇州智核生物成立于2015年���,是一家以“用最具創(chuàng)新性的核醫(yī)學診療產品�,給患者帶來新的希望”為使命的核醫(yī)藥公司�����,致力于為全球患者提供創(chuàng)新性的放射性核素診療藥物����。
智核生物創(chuàng)建了具有自主知識產權的基于單域抗體的放射性藥物發(fā)現(xiàn)、研發(fā)����、生產技術平臺,并按照cGMP標準建設并啟用了數(shù)千平的放射性藥物GMP車間(乙級資質)���。公司前瞻性地布局了10多個創(chuàng)新核素診斷和治療產品管線��。國內首個人促甲狀腺激素(rhTSH���,智舒嘉?)已獲批上市�����,將填補中國大陸用藥空白���。多個創(chuàng)新的針對腫瘤的放射性顯影藥物已經逐步進入臨床,全新靶點的放射性治療性藥物獲得潛在分子���,即將啟動臨床����。