近日,中國(guó)疫苗行業(yè)協(xié)會(huì)和中國(guó)標(biāo)準(zhǔn)化協(xié)會(huì)聯(lián)合發(fā)布了《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》團(tuán)體標(biāo)準(zhǔn)����。《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)第一起草單位為北京百奧利盟軟件技術(shù)有限公司�����,第一起草人為倪毅����。第一起草單位和起草人組織����、聯(lián)合多位權(quán)威專家共同編制《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》,第一起草單位和起草人邀請(qǐng)多位業(yè)內(nèi)權(quán)威專家對(duì)《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》進(jìn)行意見(jiàn)征集和預(yù)審��,最終形成了標(biāo)準(zhǔn)報(bào)批稿。
北京百奧利盟軟件技術(shù)有限公司創(chuàng)始人兼總經(jīng)理倪毅介紹道:”多年來(lái)�,我們始終專注于生命科學(xué)數(shù)字化領(lǐng)域,腳踏實(shí)地��,步步前行����。從服務(wù)客戶起步,到自主研發(fā)產(chǎn)品�,再到編制行業(yè)標(biāo)準(zhǔn),我們的成長(zhǎng)與行業(yè)發(fā)展緊密相連���。我們堅(jiān)信���,通過(guò)不斷完善數(shù)字化工具,我們不僅能為客戶創(chuàng)造價(jià)值�����、提供優(yōu)質(zhì)服務(wù)����,更能推動(dòng)整個(gè)行業(yè)的進(jìn)步,從而實(shí)現(xiàn)對(duì)國(guó)家生命科學(xué)領(lǐng)域的數(shù)字化轉(zhuǎn)型貢獻(xiàn)力量��。這是我們的使命,也是激勵(lì)我們不斷前進(jìn)的動(dòng)力����。”


這一標(biāo)準(zhǔn)的制定是對(duì)國(guó)家藥品監(jiān)督管理局食品藥品審核查驗(yàn)中心《細(xì)胞治療產(chǎn)品生產(chǎn)質(zhì)量管理指南(試行)》的積極響應(yīng)�����。它為細(xì)胞治療產(chǎn)品的追溯系統(tǒng)提供了具體的技術(shù)參考�����,有助于實(shí)現(xiàn)產(chǎn)品全生命周期的數(shù)字化追溯管理�。這不僅有利于落實(shí)相關(guān)法規(guī)要求��,也為行業(yè)的規(guī)范化發(fā)展提供了支持。
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)編制團(tuán)隊(duì)和預(yù)審團(tuán)隊(duì)涵蓋細(xì)胞治療領(lǐng)域和地域廣泛�,包括細(xì)胞與基因數(shù)字化專家,大型生物藥企的運(yùn)營(yíng)負(fù)責(zé)人和信息部門負(fù)責(zé)人�����、大型研究型醫(yī)院業(yè)務(wù)負(fù)責(zé)人和信息部門負(fù)責(zé)人�����、細(xì)胞治療企業(yè)負(fù)責(zé)人����。
起草人和單位
倪毅(北京百奧利盟軟件技術(shù)有限公司創(chuàng)始人/總經(jīng)理)
華堅(jiān)(上海醫(yī)藥集團(tuán)生物治療技術(shù)有限公司總經(jīng)理)
邵揚(yáng)(上海醫(yī)藥集團(tuán)信息中心主任)
衡反修(北京大學(xué)腫瘤醫(yī)院信息部主任)
沈東炎(廈門大學(xué)附屬第一醫(yī)院精準(zhǔn)醫(yī)療中心主任)
胡欣(復(fù)旦大學(xué)附屬腫瘤醫(yī)院精準(zhǔn)醫(yī)療中心主任)
羅敏(廣州百暨基因科技有限公司總經(jīng)理)
王婷婷(廣州來(lái)恩生物醫(yī)藥有限公司首席運(yùn)營(yíng)官)
預(yù)審專家(按姓氏拼音排序)
李秀玲?(上海生物制品研究所有限責(zé)任公司總經(jīng)理)
劉雅容?(沙礫生物聯(lián)合創(chuàng)始人/CEO)
羅林云?(中國(guó)生物技術(shù)股份有限公司營(yíng)銷中心副總經(jīng)理)
陸家海?(國(guó)家藥品監(jiān)督管理局疫苗及生物制品質(zhì)量監(jiān)測(cè)與評(píng)價(jià)重點(diǎn)實(shí)驗(yàn)室主任)
錢其軍?(上海細(xì)胞治療集團(tuán)董事長(zhǎng)兼CEO)
齊菲菲?(北京藝妙神州醫(yī)藥科技有限公司聯(lián)合創(chuàng)始人/CTO)
田正隆?(高博臨床研究中心首席戰(zhàn)略官兼首席數(shù)據(jù)官)
王立群(星奕昂(上海)生物科技有限公司創(chuàng)始人/董事長(zhǎng)兼CEO,副總裁袁歆代)
徐靜?(中國(guó)生物研究院副院長(zhǎng))
張丹?(江蘇譜新生物醫(yī)藥有限公司聯(lián)合創(chuàng)始人)
2023年7月 標(biāo)準(zhǔn)申報(bào)-工作組討論稿??
2023年9月 合規(guī)性審查-工作組討論稿
2024年3月 正式立項(xiàng)-征求意見(jiàn)稿
2024年3-4月 征求意見(jiàn)-征求意見(jiàn)稿
2024年4月 預(yù)審-送審討論稿
2024年5月 會(huì)審-報(bào)批稿
2024年5月 中國(guó)生物制品大會(huì)公示-報(bào)批稿
2024年6月 結(jié)束公示
2024年7月12日 中國(guó)疫苗行業(yè)協(xié)會(huì)�����、中國(guó)標(biāo)準(zhǔn)化協(xié)會(huì)聯(lián)合發(fā)布-正式文件


標(biāo)準(zhǔn)的依據(jù)法規(guī)和內(nèi)容介紹
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》依據(jù)《細(xì)胞治療產(chǎn)品生產(chǎn)質(zhì)量管理指南(試行)》第十一章產(chǎn)品追溯系統(tǒng)���,細(xì)胞治療產(chǎn)品范圍包括按藥品批準(zhǔn)上市的經(jīng)過(guò)適當(dāng)?shù)捏w外操作(如分離����、培養(yǎng)����、擴(kuò)增、基因修飾等)而制備的人源活細(xì)胞產(chǎn)品���,包括經(jīng)過(guò)或未經(jīng)過(guò)基因修飾的細(xì)胞�,如自體或異體的免疫細(xì)胞�、干細(xì)胞、組織細(xì)胞或細(xì)胞系等產(chǎn)品�����。標(biāo)準(zhǔn)適用于細(xì)胞產(chǎn)品從供者材料的采集�、運(yùn)輸、接收�、產(chǎn)品生產(chǎn)和檢驗(yàn)到成品放行、儲(chǔ)存����、運(yùn)輸和使用的全過(guò)程。
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)規(guī)定了細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)的定義�、適用范圍以及功能要求。標(biāo)準(zhǔn)適用于細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)的規(guī)劃���、設(shè)計(jì)�����、開(kāi)發(fā)�����、應(yīng)用和評(píng)價(jià)����。
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)主要內(nèi)容包括:
1. 系統(tǒng)管理:規(guī)定了用戶管理�����、角色權(quán)限����、產(chǎn)品類型�、審計(jì)追蹤等基礎(chǔ)功能��,為系統(tǒng)的安全性和可追溯性奠定基礎(chǔ)���。
2. 供者材料采集與運(yùn)輸:詳細(xì)規(guī)定了從供者材料采集申請(qǐng)到運(yùn)輸全過(guò)程的管理要求����,確保供者材料的可追溯性���。
3. 產(chǎn)品生產(chǎn):涵蓋了從供者材料接收到產(chǎn)品放行的全過(guò)程����,實(shí)現(xiàn)生產(chǎn)環(huán)節(jié)的全程可控���。
4. 產(chǎn)品存儲(chǔ)����、申請(qǐng)與運(yùn)輸:規(guī)定了產(chǎn)品入庫(kù)���、出庫(kù)����、運(yùn)輸計(jì)劃等環(huán)節(jié)的管理要求,保證產(chǎn)品流轉(zhuǎn)過(guò)程的可追蹤���。
5. 產(chǎn)品使用:包括產(chǎn)品接收���、復(fù)融和輸注等環(huán)節(jié)����,確保產(chǎn)品使用過(guò)程的安全性和可追溯性。
6. 產(chǎn)品召回:規(guī)定了產(chǎn)品召回的全流程管理���,提高了不良事件的應(yīng)對(duì)能力���。
7. 產(chǎn)品信息追溯:支持通過(guò)多種標(biāo)識(shí)碼查詢產(chǎn)品全生命周期信息,實(shí)現(xiàn)了全方位的追溯能力����。
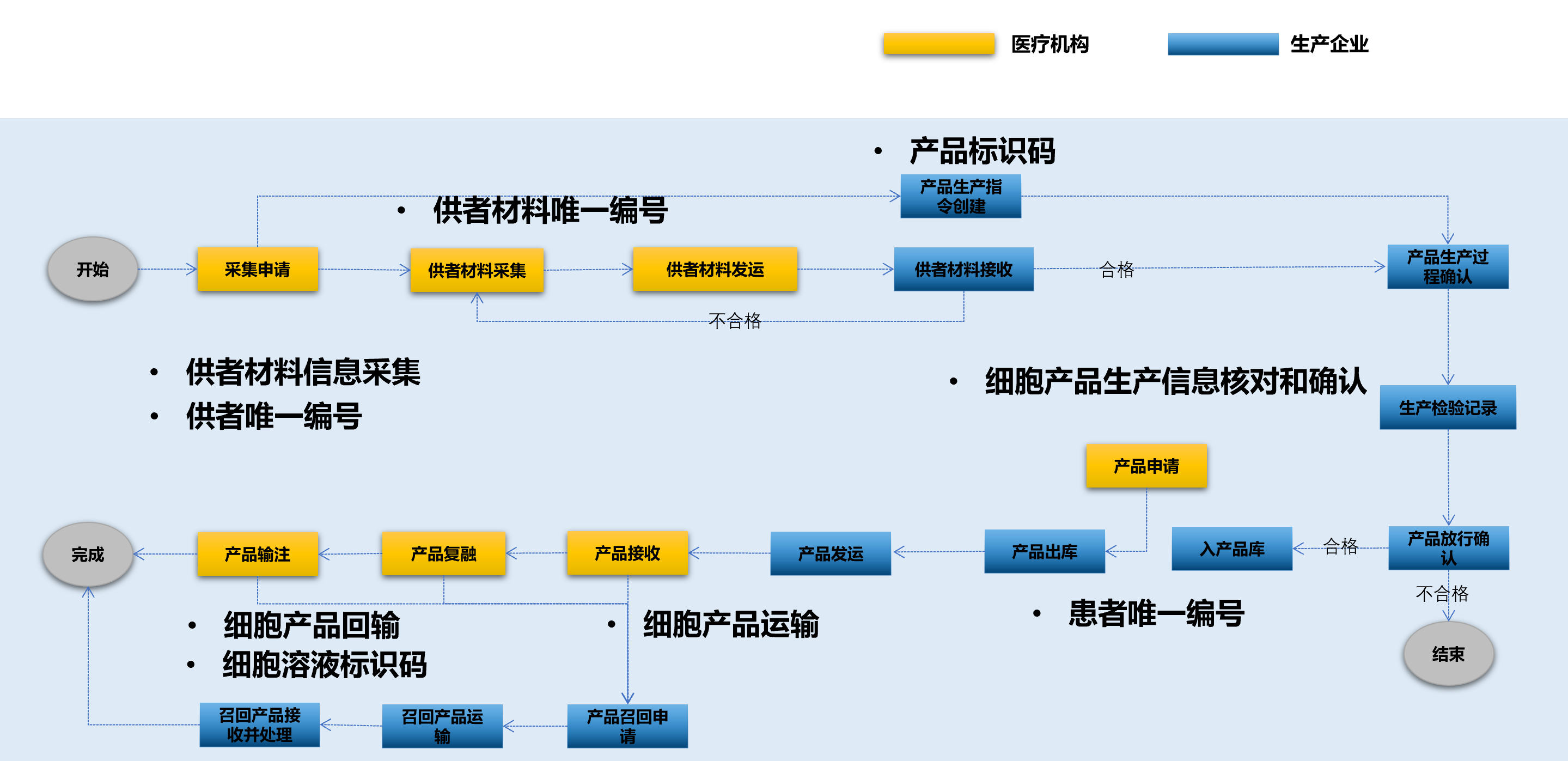
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)的發(fā)布對(duì)細(xì)胞治療產(chǎn)品追溯具有重要意義:
1. 實(shí)現(xiàn)全程可追溯:通過(guò)統(tǒng)一的信息系統(tǒng)、用于標(biāo)識(shí)供者材料和產(chǎn)品的唯一性的編號(hào)�����,實(shí)現(xiàn)從供者材料采集到產(chǎn)品使用的全過(guò)程追溯�,實(shí)現(xiàn)產(chǎn)品從供者到患者或從患者到供者的雙向追溯。
2. 實(shí)現(xiàn)數(shù)據(jù)防混淆:在從供者材料采集到產(chǎn)品使用的全過(guò)程中���,確?�?勺R(shí)別供者且具有唯一性的編號(hào)不會(huì)發(fā)生標(biāo)識(shí)錯(cuò)誤或遺漏���,確保供者材料或細(xì)胞產(chǎn)品與患者之間的匹配性。
3. 提高數(shù)據(jù)安全性:通過(guò)嚴(yán)格的身份認(rèn)證����、權(quán)限管理和審計(jì)追蹤,保障了系統(tǒng)和數(shù)據(jù)的安全性�,同時(shí)也保護(hù)了供者和患者的隱私。
4. 規(guī)范行業(yè)標(biāo)準(zhǔn):為細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)的開(kāi)發(fā)和應(yīng)用提供了統(tǒng)一的標(biāo)準(zhǔn)���,有利于行業(yè)的規(guī)范化發(fā)展���。
5. 落實(shí)法規(guī)要求:該標(biāo)準(zhǔn)源于《細(xì)胞治療產(chǎn)品生產(chǎn)質(zhì)量管理指南(試行)》,將法規(guī)要求具體化、操作化���,便于企業(yè)和醫(yī)療機(jī)構(gòu)執(zhí)行���。
6. 提升應(yīng)急能力:通過(guò)完善的召回機(jī)制,提高了對(duì)不良事件的快速響應(yīng)能力���,最大限度地保障患者安全�����。
《細(xì)胞治療產(chǎn)品追溯管理信息系統(tǒng)基本功能規(guī)范》標(biāo)準(zhǔn)的發(fā)布,是我國(guó)細(xì)胞治療領(lǐng)域質(zhì)量管理體系建設(shè)的重要一步����。這一標(biāo)準(zhǔn)為產(chǎn)品追溯系統(tǒng)提供了具體的技術(shù)參考,有助于企業(yè)更好地落實(shí)相關(guān)法規(guī)要求����。它不僅為行業(yè)提供了可操作的參考,也為提升細(xì)胞治療產(chǎn)品全生命周期的可追溯性創(chuàng)造了條件����。我們期待看到,隨著這一標(biāo)準(zhǔn)的逐步實(shí)施,細(xì)胞治療產(chǎn)品質(zhì)量管理和患者安全保障方面取得新的進(jìn)展����。