近日�����,宜聯(lián)生物YL201項(xiàng)目在2024年歐洲腫瘤內(nèi)科學(xué)會(huì)(ESMO)上公布其臨床數(shù)據(jù)����。YL201是一款靶向B7H3的ADC,基于宜聯(lián)生物TMALIN?平臺(tái)所開發(fā)�,此次報(bào)告是YL201臨床數(shù)據(jù)首次公開。
此次報(bào)告以口頭報(bào)告的形式在本次ESMO會(huì)議的Proffered Paper Session展示����,數(shù)據(jù)來自于在中、美開展的臨床I期劑量遞增和劑量擴(kuò)展研究(NCT05434234 & NCT06057922)�����。報(bào)告數(shù)據(jù)顯示��,截至2024年8月9日�,該項(xiàng)I期研究共計(jì)入組312例晚期實(shí)體瘤患者,其中包括廣泛期小細(xì)胞肺癌(ES-SCLC�,n=79)、鼻咽癌(NPC���,n=75)����,驅(qū)動(dòng)基因陰性的非小細(xì)胞肺癌(NSCLC�����,n=68)等����。所有受試者既往均接受過標(biāo)準(zhǔn)治療���,其中60%接受過2線以上治療。劑量遞增研究在0.8-3.0 mg/kg共6個(gè)劑量水平進(jìn)行�����,在2.8和3.0 mg/kg劑量組下分別觀察到1例和2例劑量限制性毒性(DLT)事件��,2.0和2.4 mg/kg被選作后續(xù)的推薦擴(kuò)展劑量�。有效性方面,截至2024年8月9日�����,在276例存在至少一次基線后腫瘤評(píng)估的患者中���,客觀緩解率(ORR)為44.6%����,疾病控制率(DCR)為83.7%���。不同腫瘤中的療效分別如下:
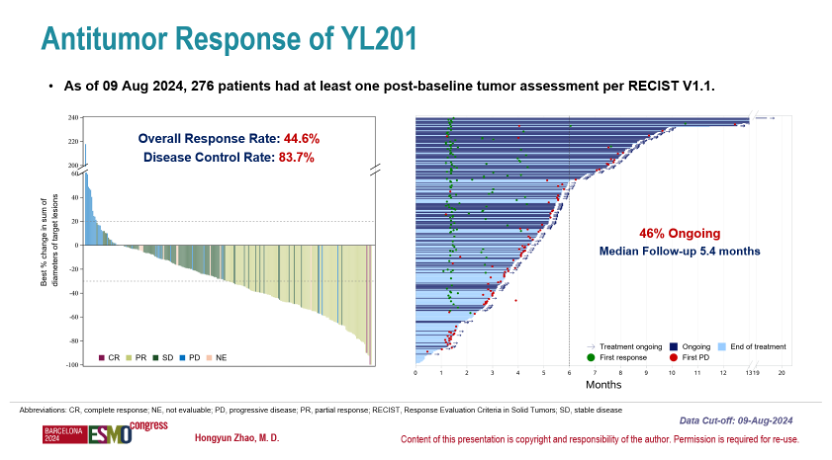
ES-SCLC隊(duì)列共計(jì)72例可評(píng)估療效的患者,既往全部接受過含鉑化療��,95%接受過anti-PD-(L)1治療��。YL201在ES-SCLC患者中的ORR為68.1%(≥2.0 mg/kg ORR為70.0%)�����,mPFS為6.2個(gè)月(≥2.0 mg/kg mPFS為6.2個(gè)月)����。值得一提的是,YL201在腦轉(zhuǎn)移患者中的療效與整體人群可比�,ORR為52.2%,mPFS為5.3個(gè)月�。NPC隊(duì)列共計(jì)70例可評(píng)估療效的患者,既往全部接受過含鉑化療和anti-PD-(L)1治療����,75%接受過2線及以上標(biāo)準(zhǔn)治療�。YL201在NPC患者中的ORR為48.6%(≥2.0 mg/kg ORR為48.6%)���,mPFS為7.2個(gè)月(≥2.0 mg/kg mPFS為7.2個(gè)月)����。在接受過2線及以上標(biāo)準(zhǔn)治療的患者中�����,ORR為51.0%���,mPFS為7.0個(gè)月��,與NPC總體人群相當(dāng)�����。驅(qū)動(dòng)基因陰性NSCLC隊(duì)列共計(jì)59例可評(píng)估療效的患者����,既往全部接受過含鉑化療和anti-PD-(L)1治療����。按病理分型來看�����,YL201在腺癌和淋巴上皮瘤樣癌(LELC)亞型中的ORR分別為29.2%和60.9%����,mPFS分別為未成熟和8.1個(gè)月�����。
安全性方面���,312例總體人群中≥G3 TRAE發(fā)生率為51%,SAE發(fā)生率為28%���。最常見的TRAE為血液學(xué)毒性�����,包括白細(xì)胞減少癥(≥G3 29%)��、貧血(≥G3 22%)��、中性粒細(xì)胞減少癥(≥G3 30%)等���;非血液學(xué)TRAE包括食欲減少(≥G3 1%)����、惡心(≥G3 1%)等�����,間質(zhì)性肺炎(ILD)僅有3例報(bào)道(1.0%)���。
“我們非常高興在ESMO大會(huì)上分享YL201的數(shù)據(jù)”�����,宜聯(lián)生物首席醫(yī)學(xué)官秦續(xù)科博士提到�?���!耙言诔?00人的樣本中所積累的數(shù)據(jù)扎實(shí)地展示了YL201項(xiàng)目在多種實(shí)體瘤的抗腫瘤效果,尤其是小細(xì)胞肺癌�、鼻咽癌、野生型非小細(xì)胞肺癌等瘤種����。YL201相比于現(xiàn)有標(biāo)準(zhǔn)治療有著顯著改善���,同時(shí)安全性良好可耐受。我們已在準(zhǔn)備小細(xì)胞肺癌���、鼻咽癌等適應(yīng)癥上的臨床III期試驗(yàn)�?!?br style="-webkit-tap-highlight-color: transparent; margin: 0px; padding: 0px; outline: 0px; max-width: 100%; box-sizing: border-box !important; overflow-wrap: break-word !important;"/>
宜聯(lián)生物成立于2020年,是一家專注于開發(fā)創(chuàng)新型偶聯(lián)藥物的臨床階段生物科技公司��。公司開發(fā)的新一代具有自主知識(shí)產(chǎn)權(quán)的腫瘤微環(huán)境可激活的新型毒素連接子平臺(tái)技術(shù)(TMALIN?)可實(shí)現(xiàn)高DAR值高均一性的穩(wěn)定偶聯(lián)�,有助于提高ADC藥物在實(shí)體瘤適應(yīng)癥上的治療窗。公司致力于以未滿足的臨床需求為目標(biāo)��,為全球腫瘤患者帶來更好的治療方案�����。宜聯(lián)生物位于中國蘇州�����,并在中國上海��、美國波士頓建立研發(fā)分支機(jī)構(gòu)��。
腫瘤微環(huán)境可激活的毒素連接子 (TMALIN?) 抗體偶聯(lián)藥物(ADC)平臺(tái)技術(shù)是宜聯(lián)生物擁有獨(dú)立自主知識(shí)產(chǎn)權(quán)的新型ADC平臺(tái)技術(shù)��,可利用細(xì)胞外腫瘤微環(huán)境和細(xì)胞內(nèi)溶酶體雙重裂解機(jī)制�,兼具高水溶性、高DAR均一性�����、高血漿穩(wěn)定性以及腫瘤組織富集的特性����。基于TMALIN?的ADC在臨床前藥效和毒理測(cè)試中展現(xiàn)出優(yōu)秀的治療窗�,目前已有多款基于該平臺(tái)的ADC產(chǎn)品進(jìn)入臨床試驗(yàn)階段。